陈良怡:下一代活细胞超分辨率成像——新原理、新应用
2021年11月6至7日,北京大学IDG麦戈文脑科学研究所成立十周年庆典暨北京大学脑科学国际论坛成功举办。来自美国哈佛大学、斯坦福大学、加州大学伯克利分校、英国伦敦大学学院、德国马普研究所、日本筑波大学、北京师范大学、中科院脑智卓越创新中心等国内外高校和科研机构的知名学者,从分子、细胞、环路、系统、认知、心理、计算、神经精神疾病等多个层面和角度,热情分享了他们在脑科学前沿研究的最新进展,并与线上线下观众频繁互动,在思维的碰撞中激荡出创新的火花。现陆续推出相关学术笔记,让我们重温精彩再出发!
本期推出的学术笔记,根据北京大学IDG麦戈文脑科学研究所、未来技术学院陈良怡教授,所作的题为“The next-generation of live-cell super-resolution microscopy: new mechanisms and new applications”的学术报告整理而成。

陈良怡教授作学术报告并与嘉宾观众交流
撰稿:邱国华
审核:陈良怡
近年来,超分辨率荧光(以下简称SR)显微镜的使用呈指数级增长,为许多生物过程提供了新的机理见解。然而,由于SR成像所需的光照度通常是以多个数量级的高于传统荧光显微镜,人们早就认识到活细胞SR显微镜技术受到光漂白和光毒性的严重限制。因此,如何实现超快SR显微成像和长时间活细胞SR显微成像的兼容是生物成像中的终极问题。为了解决上面的问题,陈良怡教授发明了两代的超灵敏SR结构光显微镜:“神机(Hessian-SIM)”和“妙算(Sparse-SIM)”。
神机(Hessian-SIM1):提高灵敏度降低光毒性
第一代是用于活细胞长期超分辨成像的海森结构光超分辨率显微镜。陈良怡教授课题组提出生命活动信号的时空连续性是生物荧光图像的通用先验知识,开发了基于Hessian矩阵(Hessian-SIM)的结构化照明显微成像的解卷积算法。在低信号强度下获得伪影最小的SR图像,所使用的光子剂量不到传统结构光超分辨率显微镜的十分之一。海森结构光超分辨率显微镜提高成像速度,降低光漂白,解决了领域内如何将超高分辨率显微镜真正应用于细胞生物学动态研究这个关键问题。利用该显微镜,第一次在活细胞中辨识出来胰岛素囊泡融合时发生的分泌孔道,并观察到线粒体内嵴的动态变化, 实现活细胞中一小时的长时间超分辨率成像。在每秒钟得到188张超高分辨率图像时,海森结构光显微镜的空间分辨率可以达到85纳米,能够分辨单根头发的1/600到1/800大小结构,而所需要的光照度小于常用的共聚焦显微镜光照度三个数量级。由于极低的光漂白以及光毒性,实现了100Hz超高分辨率成像下连续采样10分钟得到18万张超高分辨率图像,或者是在1Hz超高分辨率成像下连续1小时超高分辨率成像基本无光漂白。
与获得2014年Nobel化学奖的受激辐射损耗超高分辨率显微镜(STED)相比,海森结构光显微成像以极高的时间分辨率、极低的光毒性在活细胞超高分辨率成像方面占显著优势。例如,在观察细胞内囊泡与细胞质膜融合释放神经递质和激素过程中,海森结构光显微镜与STED显微镜(分辨率60纳米,每秒5幅左右;巫凌钢实验室2018年3月Cell上线的文章)都可以观察到囊泡融合形成的孔道;但是,海森结构光显微镜还解析出囊泡融合时四个不同中间态,包括囊泡打开3纳米小孔、囊泡塌陷、融合孔道维持和最后的囊泡与细胞质膜完全融合的过程,真正可视化膜孔道形成的全过程(图1)。
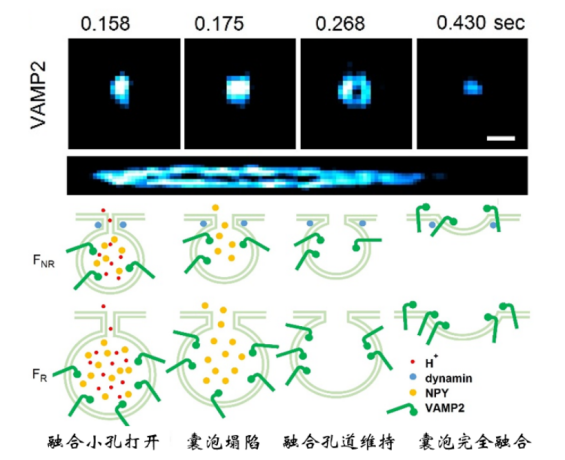
图1 海森结构光显微镜解析囊泡融合孔道形成全过程。上图:实际的动态过程解析;下图:由实验结果得到的囊泡融合的四个中间态。
妙算(Sparse-SIM2):通过计算,进一步提高活细胞超分辨率显微镜的空间分辨率
尽管理论上具有无限的空间分辨率,但活细胞成像中超分辨率显微镜空间分辨率受限于荧光分子单位时间内发出的光子数。迄今为止,基于光学硬件或者荧光探针的改进无法进一步提升活细胞超分辨率的时空分辨率,实现毫秒尺度60nm的时空分辨率成像。例如具有近60nm分辨率的非线性结构光显微镜以降低时间分辨率为代价,需使用光漂白敏感的可光活化/光开关荧光蛋白。由于细胞深层内部的分辨率和对比度仍然受到荧光发射和离焦平面散射的影响,因此高对比度超分辨结构光成像限于0.1μm~1μm的成像深度。迄今为止,没有一种超分辨方法能够在活细胞中实现约60nm时空分辨率的毫秒曝光,或者能够进行多色、三维、长期超分辨成像。
为了解决上述问题,陈良怡教授课题组基于新计算原理发明了第二代稀疏解卷积荧光超分辨率显微镜。利用“荧光图像的分辨率提高等价于图像的相对稀疏性增加”(Sparsity)这个荧光超分辨率显微成像的通用先验知识,结合之前提出的信号时空连续性(Continuity)先验知识,发明了两步迭代解卷积求解算法,即稀疏解卷积(Sparse deconvolution)方法。其中稀疏性约束恢复高频信息(朝向真实信号),同时这一重建过程也受到时空连续性的约束。这两个处于不同级别上的先验约束协同恢复信号,使得所提出的稀疏解卷积远远比只有单一约束的解卷积模型更加稳健和有效(图2)。使其能够有效鲁棒地突破现有光学显微系统的硬件限制,首次实现荧光的计算超分辨率显微成像,达到2倍左右分辨率提升。
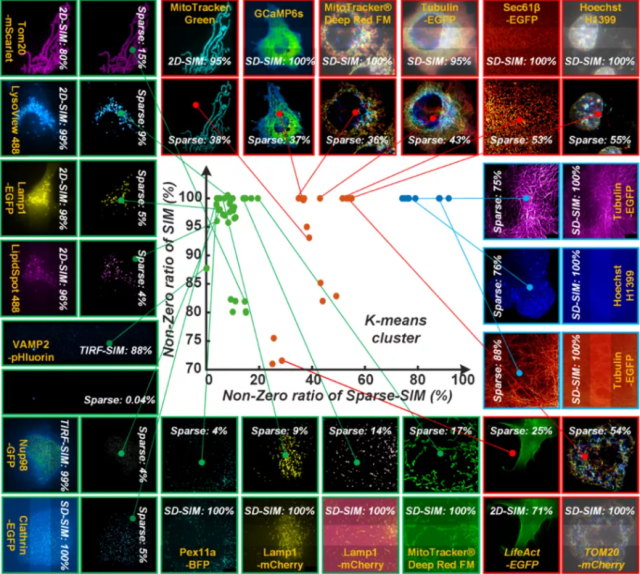
图2 稀疏解卷积广泛应用于不同模态、各类细胞器
Sparse-SIM应用举例
1. Sparse-SIM超快活细胞成像揭示胰岛素囊泡早期融合孔道
结合自主研发的超分辨率结构光(SIM)系统,Sparse-SIM能够实现目前活细胞光学成像中最高空间分辨率(60nm)下,速度最快(564Hz)、成像时间最长(1小时以上)的超分辨成像。通过滚动(Rolling)重建,在564Hz的时间分辨率下,Sparse-SIM能够识别出来INS-1细胞中VAMP2-pHluorin标记的、更小的胰岛素囊泡融合孔道(如~61nm孔径,图3o, 3p)。它们在囊泡融合的早期出现,孔径小(平均直径~87nm),持续时间短(9.5ms),不能被之前传统的TIRF-SIM所识别。

图3 Sparse-SIM解析超快胰岛素代谢过程
2. Sparse SD-SIM四色90 nm分辨率超分辨成像
结合商业的转盘共聚焦结构光显微镜(SD-SIM),Sparse SD-SIM能够实现以优于90nm的分辨率,四色、三维、长时间的活细胞超分辨成像。如图4,利用Sparse SD-SIM进行四色超分辨成像,允许在~90nm分辨率下,活细胞中,同时观测溶酶体、线粒体、微管和细胞核的动态图像。
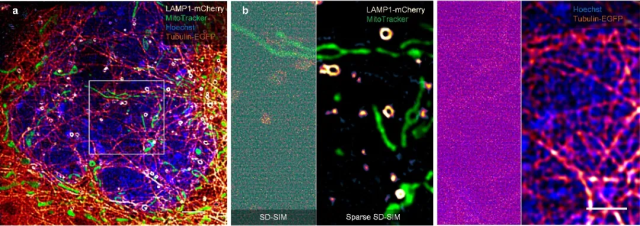
图4 稀疏SD-SIM进行四色超分辨成像
3.稀疏解卷积增强的STED活细胞成像(Sparse-STED)
同样的,稀疏解卷积技术也可以提升受激辐射损耗显微镜(STED)的空间分辨率,使用Lifeact-GFP和Sec61β-GFP在COS-7活细胞中表达后,研究人员对比了在STED下直接或经稀疏解卷积优化后成像(图5)。结果表明,使用了稀疏解卷积优化后,重建图像的FRC(Fourier ring correlation)分辨率可提升一倍左右。
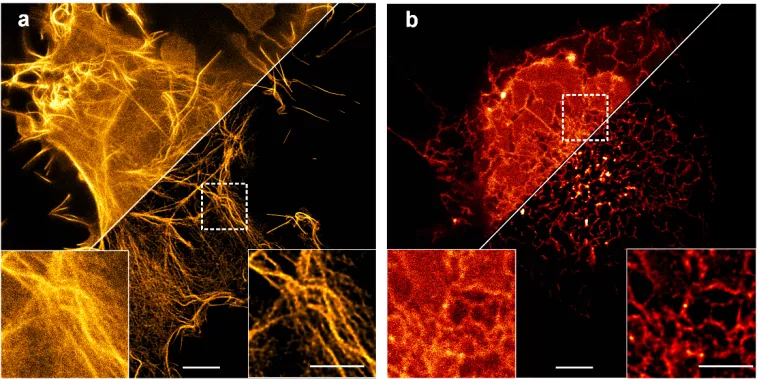
图5 利用稀疏解卷积提升STED显微镜的空间分辨率
4. Sparse MTPM记录小鼠脑部神经元树突棘的三维分布
应用微型化双光子显微成像(Sparse-MTPM)活体三维成像转基因小鼠视皮层Thy1-GFP标记的神经元树突棘(图6),深度为50~160μm。稀疏解卷积处理后可以观察到显著的频谱延展,强于传统的RL(Richardson-Lucy)解卷积(RL-MTPM),更清楚观察到树突棘三维结构。
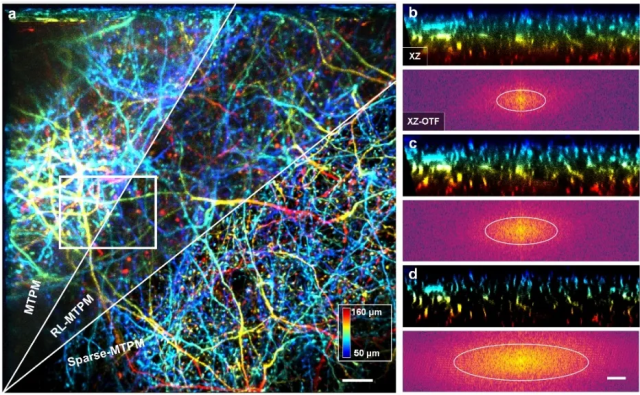
图6 稀疏解卷积技术优化微型化双光子显微镜
参考文献
[1] Huang X, Fan J, Li L, et al. Fast, long-term, super-resolution imaging with Hessian structured illumination microscopy [J]. Nature Biotechnology, 2018, 36(5): 451-459.
[2] Weisong Z, Shiqun Z, Liuju L, et al. Sparse deconvolution improves the resolution of live-cell super-resolution fluorescence microscopy [J]. Nature Biotechnology, 2021: DOI: https://doi.org/10.1038/s41587-021-01092-2.